







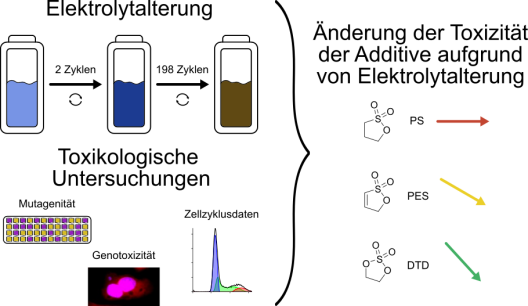
Lithium-Ionen Batterien sind aus der modernen Gesellschaft nicht mehr wegzudenken: Sie speichern die Energie in unseren Smartphones und Elektroautos und sollen in Zukunft zur Stabilisierung der Netze im Rahmen des Ausbaus erneuerbarer Energien dienen. Als mögliche Gefahren durch Lithium-Ionen Batterien ist den Verbrauchenden vor allem die Brandgefahr bekannt. Dass auch toxikologische Gefahren von den Bestandteilen ausgehen können, wird in der Literatur zwar diskutiert, allerdings meist mit Fokus auf die Elektrodenmaterialien.
Die Toxizität des am leichtesten freizusetzenden Bestandteils, des Elektrolyten, wird jedoch selten betrachtet. Aus diesem Grund untersuchte die Doktorandin Elisabeth Muschiol aus der Arbeitsgruppe von Prof. Dr. Melanie Esselen die genetische Toxizität von Elektrolyten mit drei strukturell verwandten schwefelhaltigen Additiven. Dabei wurden etablierte Testsysteme in humanen Leberkrebszellen und Bakterien verwendet, um genotoxische und mutagene Effekte auf diese Modellorganismen zu erfassen, sowie ein neues Testsystem zur schnelleren und objektiveren Erfassung der Genotoxizität im Zellkulturmodell am Institut etabliert, welches zudem zusätzliche Informationen über den Gesundheitszustand der Zellen liefert.
Die Ergebnisse des interdisziplinären Forschungsprojekts zeigten einen eindeutigen Einfluss der Alterung der Batterie auf die Toxizität der verschiedenen Elektrolyte. Es wurde deutlich, dass die unverbrauchten Elektrolyte mit 1,3,2-Dioxathiolan-2,2-dioxid (DTD) in allen untersuchten Modellen die geringste genetische Toxizität zeigten und diese außerdem mit zunehmendem Alter der Batterie weiter verringert wurde. Bei Verwendung von 1,3-Propansulton (PS) wurde sowohl im frischen, als auch in den gealterten Elektrolyten eine hohe Toxizität auf gleichbleibendem Niveau nachgewiesen. Elektrolyte mit Prop-1-en-1,3-sulton (PES) zeigten in Abhängigkeit der metabolischen Aktivität des verwendeten Testsystems zwar teils die höchste intrinsische Toxizität, aber auch eine deutliche Abnahme im Verlauf der Alterung.
Aus toxikologischer Perspektive ist somit DTD von diesen schwefelhaltigen Additiven am besten für den Einsatz in Lithium-Ionen Batterien geeignet. Die Ergebnisse wurden open access in Archives of Toxicology (https://doi.org/10.1007/s00204-025-04246-2) veröffentlicht.
Das Projekt wurde von der Internationalen Forschungsschule BACCARA, gefördert vom Ministerium für Kultur und Wissenschaft des Landes NRW, ermöglicht.
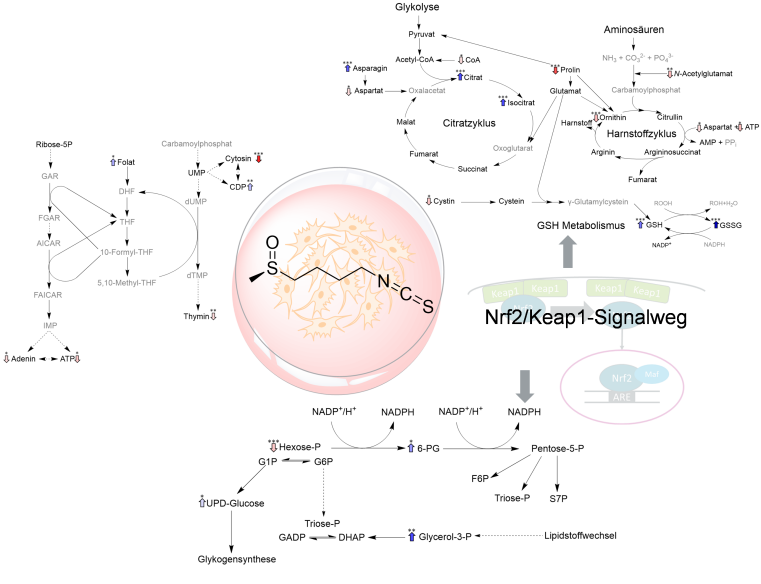
Der Verzehr von Gemüse aus der Familie der Kreuzblütler, wie z.B. Brokkoli, steht im Zusammenhang mit einer gesunden Ernährung. Kreuzblütler enthalten schwefelhaltige sekundäre Pflanzenstoffe, die sogenannten Glucosinolate, die bei der Zubereitung und auch durch den Verzehr von Kreuzblütlergemüse zu Isothiocyanaten abgebaut werden. Im Fall von Brokkoli wird der Vorläufer Glucoraphanin zu dem Isothiocyanat Sulforaphan abgebaut. In der Literatur wird Sulforaphan hinsichtlich seiner möglicherweise gesundheitsfördernden Eigenschaften diskutiert. Um tiefere Einblicke in die genaue Wirkung von Sulforaphan zu bekommen, untersuchte die Doktorandin Nadine Bieß aus der Arbeitsgroppe von Herrn Prof. Dr. Hans-Ulrich Humpf die Auswirkungen dieser Substanz auf den zellulären Stoffwechsel. Hierzu wurden Leberkrebszellen als Modellorganismus mit Sulforaphan behandelt und mittels hydrophiler Interaktionschromatographie mit massenspektrometrischer Analyse von mehr als 100 Stoffwechselprodukten die Veränderungen in den Hauptstoffwechselwegen erfasst. Dabei wurde die bestehende Methodik erweitert, um besonders instabile schwefelhaltige Stoffwechselprodukte besser nachweisen zu können.
Die Ergebnisse zeigten, dass Sulforaphan vielfältige Effekte auf mehrere Hauptstoffwechselwege hat. Ein Anstieg der antioxidativen Stoffwechselprodukte wurde beobachtet und unterstützt damit die viel diskutierte Annahme, dass Sulforaphan die zelluläre Abwehr gegen oxidativen Stress anregt. Des Weiteren konnten Einflüsse auf die Stoffwechselwege gezeigt werden, die für die Energiegewinnung zuständig sind. Ebenso wurden Veränderungen im Stoffwechsel der Aminosäuren beobachtet. Diese Ergebnisse tragen dazu bei, ein tieferes Verständnis für die Auswirkungen von Sulforaphan auf den zellulären Stoffwechsel zu erlangen. Die Studienergebnisse wurden in der Zeitschrift Molecular Nutrition and Food Research (https://doi.org/10.1002/mnfr.70373) veröffentlicht.

Am 29. November fand im großen Hörsaal des Pharma Campus die Verleihung der Abschlusszeugnisse an die Absolventinnen und Absolventen der Master-Studiengänge im Fachbereich Chemie und Pharmazie statt. Mit dabei war, wie in jedem Jahr, auch die Lebensmittelchemie. Nach einem kurzweiligen Festvortrag von Prof. Dr. von Delft erfolgte die Überreichung der Masterzeugnisse durch den Dekan Prof. Dr. Langer sowie die Verleihung der Studienpreise. Im Anschluss konnten die Absolventinnen und Absolventen bei einem Sektempfang mit ihren Familien und Mentoren auf den erfolgreichen Studienabschluss anstoßen.

Im Rahmen der Veranstaltung wurde auch der Studienpreis für die beste Masterarbeit im Fach Lebensmittelchemie an der Universität Münster überreicht. Der von der Firma ALS Germany GmbH gesponsorte und mit 1000 € dotierte Preis wurde in diesem Jahr an Stephanie Rochau verliehen.
Ihre Masterarbeit mit dem Titel "Untersuchungen zu mikrobiologischen Prozessen in
Aktivkohlefiltern bei der Aufbereitung von Trinkwasser" wurde am Institut für Molekulare Mikrobiologie und Biotechnologie unter der Betreuung von Prof. Dr. Bodo Philipp in Zusammenarbeit mit dem Institut für Lebensmittelchemie der Universität Münster durchgeführt.


Mykotoxine sind sekundäre Stoffwechselprodukte von Schimmelpilzen und wichtige Lebensmittelkontaminanten. Eine hohe Exposition gegenüber Mykotoxinen kann beispielsweise das Risiko von Krebserkrankungen erhöhen oder die Entwicklung von Kindern negativ beeinflussen. Über die Bestimmung der individuellen Mykotoxin-Belastungen beim Menschen, können diese Risiken abgeschätzt, Zusammenhänge mit auftretenden Einflüssen auf die Gesundheit erkannt und gegebenenfalls Maßnahmen zur Reduzierung der Exposition abgeleitet werden. Durch den Verzehr kontaminierter Nahrungsmittel gelangen Mykotoxine in den menschlichen Organismus, wo sie teilweise verstoffwechselt und über den Urin ausgeschieden werden. Die Exposition gegenüber Mykotoxinen lässt sich so über die Bestimmung dieser sogenannten Biomarker im Urin berechnen. Dabei sind viele Proben einer Bevölkerung nötig, um verlässliche Werte zu erhalten. Daher müssen analytische Methoden zum Nachweis von Mykotoxin-Biomarkern einen hohen Probendurchsatz gewährleisten, also zahlreiche Analysen in möglichst kurzer Zeit ermöglichen. Aufgrund der meist sehr geringen Mykotoxinkonzentrationen sowie der strukturell sehr unterschiedlichen Mykotoxine stellen sich dabei zusätzliche analytische Herausforderungen.
Im Rahmen eines aktuellen Forschungsprojektes wurde im Arbeitskreis von Prof. Dr. Hans-Ulrich Humpf durch Michael Kuhn eine neue Methode basierend auf einer automatisierten Festphasenextraktion (online solid phase extraction, online SPE) entwickelt, um diese Anforderungen zu vereinen. Die online SPE war direkt mit einer weiteren flüssigchromatographischen Trennung mit massenspektrometrischer Detektion gekoppelt. Die Urinprobe wurde dabei direkt mittels online SPE in mehreren Schritten aufgereinigt und die gewünschten Analyten aufkonzentriert. Dadurch konnte eine hohe Sensitivität der Methode erzielt und gleichzeitig der manuelle Aufwand der Probenaufarbeitung minimiert werden. Eine spezielle Verdünnung des online SPE Eluats ermöglichte die Messung der sehr polaren Analyten Deoxynivalenol und den Deoxynivalenol-glucuroniden, zusammen mit weiteren unpolaren Mykotoxinen. Insgesamt konnten 36 Mykotoxine und Mykotoxin-Metaboliten in die Methode eingefügt werden. Die Leistungsfähigkeit der neu entwickelten Nachweismethode wurde anhand von 50 Urinproben aus Bangladesch demonstriert. Neben der Analyse mittels online SPE wurden die Proben auch nach einfacher Verdünnung und ohne weitere Probenaufbereitung (dilute and shoot) untersucht. Der Vergleich der Ergebnisse beider Verfahren zeigte, dass die online SPE Methode 304% mehr positiver Befunde ermöglichte. Insgesamt wurden 15 verschiedene Mykotoxine und deren Metaboliten in den Proben gefunden.
Dank der niedrigen Nachweisgrenzen, der reduzierten manuellen Probenvorbereitung und des großen Analytumfangs stellt der online SPE-Ansatz eine leistungsstarke Methode zur zuverlässigen Abschätzung der Mykotoxinexposition dar. Die Ergebnisse wurden open access im Microchemical Journal (https://doi.org/10.1016/j.microc.2025.115821) veröffentlicht.
Das Forschungsprojekt wurde von der Deutschen Forschungsgemeinschaft gefördert (INST 211/1043–1 FUGG).
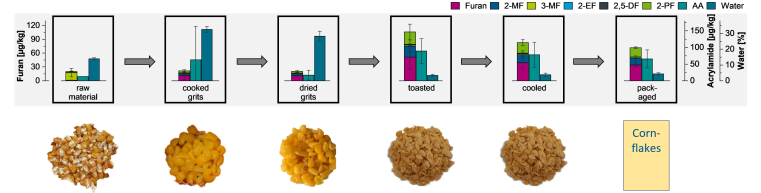
Furane sind Schadstoffe (Kontaminanten), die bei der thermischen Verarbeitung von Lebensmitteln gebildet werden können. Beispiele sind das Backen, Toasten, Frittieren oder Puffen von Lebensmitteln. Moderne Herstellungsverfahren von Frühstückscerealien umfassen oft mehrere Koch- oder Erhitzungsschritte, die einen Einfluss auf die Bildung von Furanen haben können. Welcher Prozess dabei wie stark zur Bildung von Furanen und Acrylamid, einer weiteren Kontaminante, beiträgt, wurde in einem Kooperationsprojekt mit verschiedenen Herstellern von Frühstückscerealien untersucht. Ziel des vom Bundesministerium für Wirtschaft und Energie geförderten Projekts (AIF 21305 N) war es, durch diese Untersuchungen neue Strategien zur Minimierung der Bildung von Furanen zu entwickeln.
Durch die Analyse von Rohstoffen, Zwischenprodukten und Endprodukten aus industriellen Produktionslinien konnten wir zeigen, wie stark sich die einzelnen Verarbeitungsschritte auswirken und an welchen Stellen Anpassungen der Prozessbedingungen sinnvoll sein können. Die Ergebnisse dieser Untersuchungen wurden nun in der Zeitschrift Food Control mit dem Titel „Formation of furan, alkylfurans and acrylamide during breakfast cereal manufacturing: Comparison of model experiments with industrial processes“ veröffentlicht. Beispielhaft ist hier die Bildung von Furanen und Acrylamid während der Cornflakes-Herstellung gezeigt.

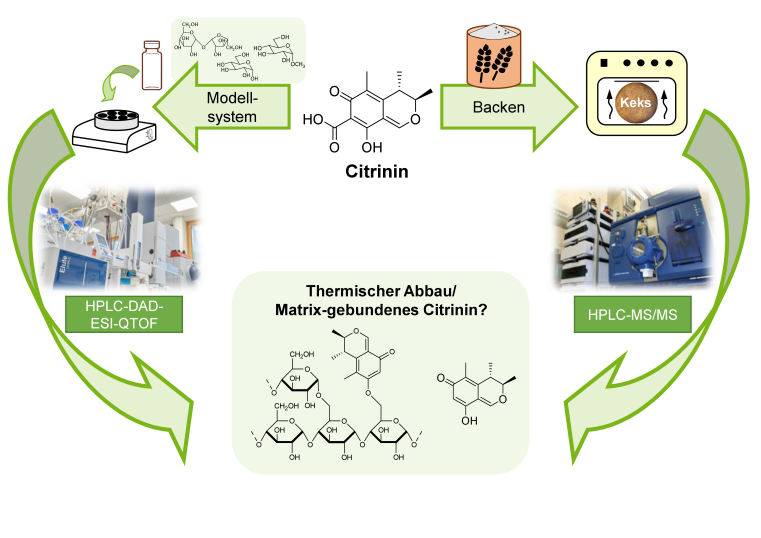
Citrinin ist ein Giftstoff (Mykotoxin) von Schimmelpilzen, das in verschiedenen Lebensmitteln, insbesondere in Getreideprodukten, vorkommt. Es wird während des Wachstums der Pflanze auf dem Feld, aber vor allem während der Lagerung, gebildet. Analysen haben gezeigt, dass der Gehalt an Citrinin in unverarbeitetem Getreide deutlich höher ist als in Endprodukten. Die Reinigung von Getreide kann diese Abnahme nur teilweise erklären, sodass Citrinin möglicherweise auch bei der thermischen Verarbeitung (Backen etc.) abgebaut wird.
Lea Brückner aus der Arbeitsgruppe von Herrn Prof. Dr. Hans-Ulrich Humpf untersuchte im Rahmen ihrer Promotion die Reaktionen von Citrinin bei der thermischen Verarbeitung von Lebensmitteln. Ziel war es, zu verstehen, was mit Citrinin bei diesen Prozessen passiert und ob das "Verschwinden" auch mit einer Abnahme der potenziell gesundheitsschädlichen Wirkung von Citrinin einhergeht. Nach ersten Studien zur Reaktion von Citrinin mit Proteinen, die bereits im vergangenen Jahr in der Zeitschrift Mycotoxin Research veröffentlicht wurden (https://doi.org/10.1007/s12550-024-00557-y), konnte Lea nun zeigen, wie Citrinin mit Zuckerstrukturen reagieren kann. Ausgehend von Modellverbindungen leitete sie einen potenziellen Reaktionsmechanismus zur Bildung von Citrinin-Zuckerkonjugaten ab. Für die Übertragung auf echte Lebensmittel und Backprozesse gelang es ihr, eine Aufarbeitung mit enzymatischer Hydrolyse zu entwickeln, die es ermöglichte, diese Verbindungen auch in realen Lebensmitteln nachzuweisen. Darüber hinaus untersuchte sie Einflussfaktoren auf die Bildung eines weiteren Reaktionsproduktes von Citrinin, Decarboxycitrinin. Durch Zellkulturexperimente konnten zudem erste Daten zur Toxizität des gebildeten Decarboxycitrinins gewonnen werden. Die Ergebnisse dieser Studien sowie die Entwicklung der Analysemethode wurden nun open access in der Zeitschrift Toxins publiziert (https://doi.org/10.3390/toxins17020086).
Das Forschungsprojekt wurde von der Deutschen Forschungsgemeinschaft gefördert (HU 730/14-1).
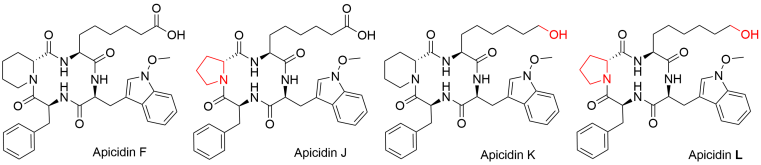
Das Grundgerüst der Apicidine besteht aus vier Aminosäuren, die in einem Ring zusammengeschlossen sind. Sie werden von verschiedensten Gattungen des Fusarium gebildet und sind vor allem für ihre Wirkung gegen den Malaria-Parasiten Plasmodium falciparum bekannt. Diese beruht auf der Inhibierung von Histondeacetylasen, welche die Verfügbarkeit der DNA für die Transkription beeinflusst und sich somit auf diverse zelluläre Signalwege auswirkt.
Bereits in der Vergangenheit wurde am Institut für Lebensmittelchemie an dem pathogenen Fadenpilz Fusarium fujikuroi gearbeitet. Damals wurden nach genetischer Modifikation des Wildtyps drei bis dahin unbekannte Apicidine charakterisiert: Apicidin F, J und K. Dabei stellte sich heraus, dass Apicidin J und K Strukturderivate von Apicidin F sind, die sich lediglich in einer Aminosäure im Ring unterscheiden. Diese Arbeit wurde nun von Alica Fischle, Doktorandin in der Arbeitsgruppe von Frau Dr. Svetlana Kalinina, weitergeführt. Hierzu wurden zunächst genetische Mutanten erzeugt und im Hinblick auf ihre Kultivierbarkeit und das Vorkommen eines weiteren Derivates untersucht. Dieses sollte beide Modifikationen, die in Apicidin J und K nachgewiesen wurden, tragen. Nach Optimierung der Kulturbedingungen wurde die Substanz zusammen mit den bekannten Apicidinen extrahiert und isoliert. Die Strukturaufklärung erfolgte mittels Kernspinresonanzspektroskopie (NMR) und hochaufgelöster Massenspektrometrie (HRMS), welche die Identität des neuen Tetrapeptids als „Apicidin L“ erfolgreich bestätigten. Des Weiteren wurde die Zelltoxizität aller vier Apicidine bestimmt und ihre biologische Aktivität in Bezug auf P. falciparum und die Inhibierung von Histondeacetylasen untersucht. Dabei wurde festgestellt, dass die Unterschiede in den Strukturen auch verschiedene Effekte in den biologischen Systemen hervorriefen. Die vollständigen Untersuchungen stehen als open access in der Zeitschrift Journal of Natural Products and Bioprospecting und unter https://doi.org/10.1007/s13659-024-00473-9 zur Verfügung. Außerdem wurde das Projekt bereits im Forschungsstadium im Rahmen des ACS Symposium: Biological and Medicinal Chemistry im März 2023 mit einem Posterpreis ausgezeichnet und ist unter https://axial.acs.org/biology-and-biological-chemistry/poster-prize-winners-acs-publications-symposium-biological-and-medicinal-chemistry einsehbar.