Dynamische Zellkontakte
Während der Angiogenese bilden sich Blutgefäße aus bereits bestehenden Gefäßen, zum Beispiel, wenn sich ein Organismus entwickelt oder wenn Wunden heilen. Bei einigen Krankheiten können ebenfalls neue Gefäße sprießen, deren Wachstum allerdings nicht dem normalen Ablauf entsprechen – zum Beispiel, wenn sich Tumoren bilden. Die innere Wand von Blutgefäßen besteht aus Endothelzellen. Entwickelt sich ein neues Gefäßnetz, bewegen sich diese Zellen, um sich neu anzuordnen. Dabei müssen sie auch ihre Kontakte mit benachbarten Zellen neu formen. Aber wie funktioniert das genau? Und wie wandern die Zellen letztendlich zielgerichtet vorwärts? Wissenschaftler des Exzellenzclusters „Cells in Motion“ (CiM) der Universität Münster haben eine Reihe molekularer Mechanismen entschlüsselt, die dahinterstecken. Sie präsentieren ein System, bei dem der gestreckten Form von Endothelzellen während der Angiogenese eine hohe Bedeutung zukommt. Eine wichtige Funktion hat außerdem das Zellkontakt-Protein VE-Cadherin, das den Zusammenhalt von Endothelzellen untereinander sicherstellt. „Unsere Ergebnisse liefern eine solide Grundlage für ein Modell, mit dem wir die Mechanismen des Zusammenspiels von VE-Cadherin und dem Zellskelett in der Angiogenese erklären können“, sagt Erstautorin Dr. Jiahui Cao. Die Studie ist aktuell in der Fachzeitschrift „Nature Communications“ erschienen.
Die Geschichte im Detail:
Verantwortlich dafür, dass neue Blutgefäße wachsen können, ist das Protein VEGF. Es dient als Signalstoff und beeinflusst zum Beispiel, dass neue Endothelzellen in eine Wunde einwandern. Um zu beobachten, wie sich Endothelzellen und ihre Kontakte zueinander während der Angiogenese verhalten, untersuchten die Forscher mit Blutgefäßen durchzogene Netzhäute von sich entwickelnden Mäusen. Außerdem sahen sie sich Kulturen aus Endothelzellen an, die sie menschlichen Nabelschnurvenen entnommen und dem Signalstoff VEGF ausgesetzt hatten. Mit verschiedenen lichtmikroskopischen Verfahren beobachteten sie die Dynamik der Zellkontakte.
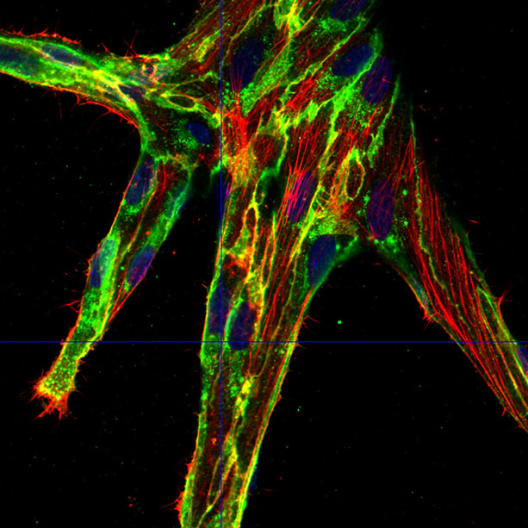
Hierzu markierten die Wissenschaftler um CiM-Gruppenleiter Prof. Dr. Hans-Joachim Schnittler zunächst das Protein VE-Cadherin auf den Endothelzellen mit fluoreszierenden Farbstoffen. Dieses Protein wirkt quasi wie ein Klettverschluss zwischen ihnen. Es steht in engem Wechselspiel mit dem Zellskelett, insbesondere mit dessen Bestandteil Aktin. Bereits in einer früheren Studie hatten die Wissenschaftler herausgefunden: Verändert eine Zelle ihre Form und erhöht ihren Umfang, kommt es zu einer verminderten Konzentration von VE-Cadherin an den Zellkontakten. Das führt dazu, dass sich Membranfortsätze aus Aktinfasern an den Zellkontakten bilden, die bewirken, dass sich die Kontakte dynamisch verändern können. Diese Zellfortsätze werden JAILs genannt – eine Abkürzung des englischen Fachbegriffs „junction-associated intermittent lamellipodia“.

Die Forscher nahmen an, dass der Mechanismus auch während der Angiogenese eine Rolle spielt und beobachteten: Endothelzellen, die sich aufgrund des erhöhten Vorkommens von VEGF streckten, wiesen einen größeren Umfang und gleichzeitig längere Zellkontakte auf. Die Menge des Proteins VE-Cadherin auf der Oberfläche einer verlängerten Endothelzelle erhöhte sich insgesamt nicht, sondern blieb gleich hoch – an den einzelnen Zellkontakten trat allerdings durch die Streckung der Zellen weniger VE-Cadherin auf als zuvor. Die Wissenschaftler fanden heraus, dass sich an den Kontaktstellen, an denen sich wenig VE-Cadherin befand, JAILs bildeten, die mit anderen Zellen überlappten und so wiederum neue Kontaktstellen für VE-Cadherin hervorriefen. Darüber hinaus belegten die Wissenschaftler, dass der Proteinkomplex Arp 2/3 aktiv sein muss, um JAILs zu bilden. Dieser Proteinkomplex spielt eine wichtige Rolle bei der Bildung von Aktinfasern und wird seinerseits durch bestimmte Proteine reguliert.
Interessanterweise entdeckten die Forscher diese dynamischen Veränderungen der Zellkontakte vor allem an den in Wanderungsrichtung ausgerichteten Positionen von Zellen. Es bildete sich ein großer JAIL, mit dem die Zelle zielgerichtet wandern konnte. Neue Kontaktstellen von VE-Cadherin wirkten dabei wie Anker, die sich an ihrer Umgebung festhalten konnten. Gleichzeitig bildeten sich kleine JAILs an der Seite der Zelle. Durch sie konnte sich eine angehängte, benachbarte Zelle mit fortbewegen. Die Wissenschaftler identifizierten noch zwei weitere hierfür wichtige Faktoren: Zum einen das Protein Rac. Bereits zuvor war bekannt, dass es für die Bildung von Fortsätzen an Zellkontakten verantwortlich ist. Das konnten die Wissenschaftler auch in ihrer aktuellen Studie nachweisen: Hemmten sie das Protein, bildeten sich keine JAILs.
Gleichzeitig entdeckten die Forscher einen Spannungsverlust der Aktin- und Myosinfilamente an den Zellkontakten, wodurch sich die Zellen strecken konnten. Dabei löste eine Reihe aufeinanderfolgender Signale den Spannungsverlust aus: Das Protein VEGF band an ein Enzym, das seinerseits die Aktivität eines weiteren Enzyms, der Myosin-leichte-Ketten-Kinase II, auslöste. Außerdem beobachteten die Wissenschaftler, dass sich Mikrotubuli, ebenfalls Bestandteile des Zellskeletts, an den Zellkontakten neu anordneten, was zusätzlich zum Spannungsverlust und zu einer höheren Dynamik an den Zellkontakten beitrug.
Die Ergebnisse könnten auch für die Erforschung von Krankheiten relevant sein – zum Beispiel, um später Medikamente zu entwickeln, welche diese molekularen Mechanismen beeinflussen. Ob und wann sich die Ergebnisse der Grundlagenforschung in möglichen Anwendungen niederschlagen, ist derzeit jedoch nicht absehbar. In der Zukunft wollen die Wissenschaftler zunächst die einzelnen signalgebenden Mechanismen weiter untersuchen, um mehr darüber zu erfahren, wie sie sich gegenseitig aktivieren, hemmen und welche Bedeutung die JAILs bei krankhaften Gefäßveränderungen haben.
Zusammenarbeit verschiedener Forschergruppen
An der Studie arbeiteten verschiedene Arbeitsgruppen des Exzellenzclusters zusammen. Die CiM-Forschergruppe um Entwicklungsbiologe Prof. Dr. Ralf Adams ist darauf spezialisiert, die Angiogenese in der Netzhaut von Mäusen zu untersuchen und erforschte das Vorkommen von VE-Cadherin in genetisch veränderten Tieren. Die Forschergruppe um Zellbiologe Prof. Dr. Erez Raz untersuchte die Aktivität des Proteins Rac mit einer speziellen Technik, dem Fluoreszenz-Resonanzenergietransfer. Darüber hinaus war eine Forschergruppe aus Prag beteiligt, die sich mit künstlicher Intelligenz befasst. „Die Zusammenarbeit mit den anderen Forschergruppen war extrem offen und die Diskussion der Ergebnisse sehr gewinnbringend“, sagt Mediziner Prof. Hans-Joachim Schnittler.
Die Studie erhielt finanzielle Unterstützung des Exzellenzclusters „Cells in Motion“ der Universität Münster, der Deutschen Forschungsgemeinschaft, des Bundesministeriums für Bildung und Forschung und der Czech Science Foundation.
Originalpublikation:
Cao J, Ehling M, März S, Seebach J, Tarbashevich K, Sixta T, Pitulescu ME, Werner A-C, Flach B, Montanez E, Raz E, Adams RH, Schnittler H. Polarized actin and VE-cadherin dynamics regulate junctional remodelling and cell migration during sprouting angiogenesis. Nat Commun 2017; 8; DOI: 10.1038/s41467-017-02373-8. Abstract

